����ϸ������Ļ���
1���������
�����°�����������ε�������ϸ�������أ�ϸ������Ļ��������ǡ�ԭ����������ɡ�������
 ԭ�������방���� ԭ�������방����
��������Դ��ԭ�������ͻ�䣺����������£�ϸ���ڴ������방֢�йصĻ�����Щ��������������Ǹ��巢����ϸ����ֳ����֯���������������ȱ�ٵġ���Щ����ֻ�з���������ṹ�ϵ����仯ʱ�����°����ã���ɰ�����(oncogene��onc)����Щ��������ϸ������DZ�ܵĻ����Ϊԭ������proto-oncogenes����ԭ�������������Ի���λ�����е�һ������ͻ�䣬�ͻ�����ϸ������,ԭ����������ֱ仯��Ϊԭ������ļ������ϸ������Ȼ������ԭ��������ԭ������Ļ�ܵ��ϸ�ľ��ܵ��أ�����������ϸ�������ͷֻ�������ģ��������𰩱䡣
ϸ��ԭ���������൱���ص�DNA˳�ӽ�ĸ����Ӭ���ˣ�ͬһ��ԭ�������DNA˳��ʮ�����ƣ������Ϊ���ܼһ���ԭ�������ڸ��巢����ϸ���ֻ���һ����ʮ����Ҫ�����ڳ����ƽʱȴ�����������ܵ��ϸ�Ŀ��ơ�Ȼ��������ӿ��Լ��������״̬��ԭ������ʹ����ͻ���Ϊ��İ����Ӷ����������ת¼�����°���Ϣ��mRNA���ϳɳ�����ת�����ף���ͨ������ø��Ϣ����ϵͳ��ʹϸ���������䡣
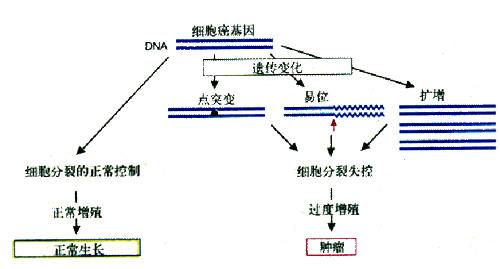
ͼ2-12ԭ������ļ������
ԭ��������ƣ�ԭ��������Ļ��ƿ������������֣�
�ٵ�ͻ�� ras��������ļ�������������ַ�ʽ���ڽ᳦�����ΰ������ٰ��Ͱ��װ���ͨ�������Է�����ras����������ͻ�䣬����ijһ�ض�λ���ϵ�������ĸı䡣���罫���װ�����������ϸ���е�ԭ��������Ƚϣ�������һ�������������ͻ�䣺����p21ras���Ļ����ڵ�һ�������ӵĵ�12����������������GGCת��ΪGTC�����¸ʰ��ᱻ�Ӱ����滻��������RAS����GTPø���ԣ����ʹϸ���°���θ������õ��Ļ������Ҳ����һ����������˸ı䡣
�ڻ������ 20����80���������������������Ӳ���ģ�ͣ�������Ϊ����ԭ�����������˲������������������Ӷ�������Ӷ��������ijЩRNA�������������а������䷴ת¼��DNA��������������ϸ����������䳤ĩ���ظ�˳��LTR����һ����ǿ�������ӣ�һ��LTR�����ͬʱ������ǿ��ͬʱ��������ϸ��ԭ��������ڲ�����ػ�������ʹԭ�����������İ����������ʵı仯�������ڲ��������������γ��йصĵ����ʿɵ���ϸ���Ķ���ת����
�ۻ������� ���������ϸ���е�ԭ������ֻ��1��2������������������ԭ������������ʮ���������ٱ���������������ɻ����һ����������������ϸ������ʱ���������Ⱦɫ�����Ⱦ����homogenously stained region��HSR���ͷdz�С�ij�˫������˿��Ⱦɫ�壬���߳�Ϊ˫�壨double minute chromosomes��DMs�������������Ļ�����ϸ��ˮƽ�ϵı��֡�������ijЩ����ϸ����c��myc�������������������ǧ����ϸ�����������������ӻ������Ե����ӣ��ǰ�������������Ľ����ʹ����ת¼ˮƽ������ϸ���иߵö࣬Ҳ�ǵ���ϸ�������ԭ��֮һ������ijЩ�����г���3��ras��c-myc�����ﵰ����������ʮ�����ϰٱ�����Ѫ�����᳦��ϸ��������ԭ�������������ת¼������������RNA�͵����ʣ����¹���ĵ����źų���������ϸ���ˣ�����ϸ�����١�������ֳ��
�ܻ������� ���ֻ���ļ��ʽ������Ⱦɫ����λ�����������ţ�ʹ������ĵ���ϵͳ�����ı��������쳣���������������ϸ����Ѫ������ϸ��������22��Ⱦɫ����9��Ⱦɫ��֮����λ�γ�phȾɫ�壬��ʹ�������c-abl��������λ�õĸı�����±����쳣�������ĵ������ܴٳ�ϸ���Ķ���ת���� | 
 ��һ��������
��һ��������